Loote rabdomüoomid koos tuberoosse skleroosse kompleksiga
Loote rabdomüoomid koos tuberoosse skleroosse kompleksiga
Eesti Naistearstide Seltsi Teataja (oktoober 2010)
Marek Šois1, Ervin Saik2, Pille Saik3, Tiiu Jalas2, Rabich Chaoui3, Stanislav Ovroutski4
1Fertilitas; 2Tallinna Lastehaigla; 3Lääne-Tallinna Keskhaigla Naistekliinik; 4Prenatal Diagnosis and Human Genetics Center Berlin,Germany; 5German Heart Institute, Berlin, Germany.
Võtmesõnad
Loote südame rabdomüoom. Tuberoosne skleroosne kompleks. Diagnostika.
28-aastane terve esmasrase, perekonnaanamnees iseärasuseta. 23. rasedusnädalal tehtud ultraheliuuringul südame leid iseärasusteta. Patsient pöördus ultraheliuuringule omal soovil uuesti 30. rasedusnädalal. Südame 4. kambri vaatel ilmestuvad loote mõlema vatsakese seintes hulgaliselt selgete piirjoontega südamelihasest ehhogeensemad ümarad kolded, mis võlvuvad vatsakeste õõnsustesse.
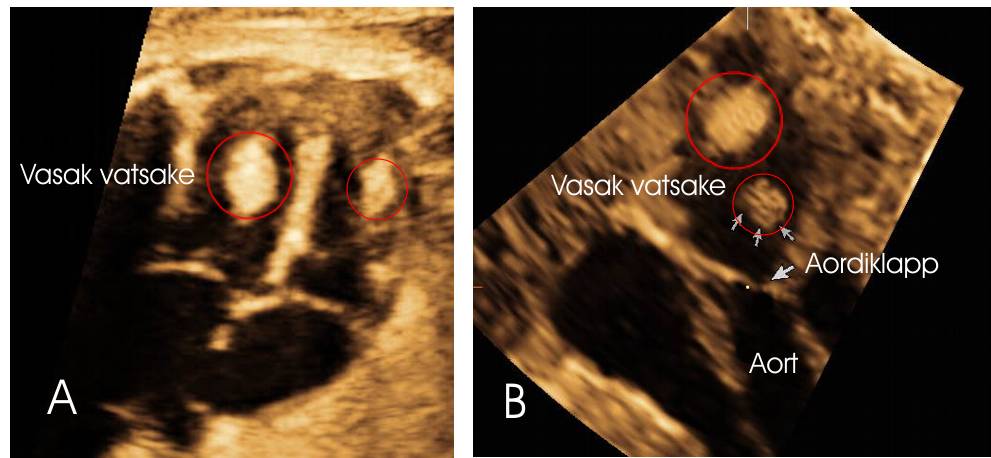
Joonis 1. A: Südame neljakambri tasapind. Nii vasaku kui ka parema vatsakese seintes visualiseeruvad tumoroossed ehhogeensed selgepiirilised ovaalsed kolded. B: Vasaku vatsakese väljutustrakti tasapind. Distaalse tuumori kaugus aordiklapist.
Suurim kolle on vasaku vatsakese seinas diameetriga 7,3 mm, paremas vatsakeses on kaks suuremat kollet, mõlema diameeter 5 mm. Südame vatsakeste vahesein oli ehhogeensem ja paksenenud. Kuigi vasaku vatsakese üks kolletest oli aordiklapile suhteliselt lähedal, ei põhjustanud see kliiniliselt vasaku väljutustrakti obstruktsiooni ega südamepuudulikkust. Südame löögisagedus varieerus 142–148 korda minutis.
Loote parenhümatoossed elundid – maks, põrn ja neerud – ilma koldeleiuta.
Loote aju aksiaalsel ja koronaarsel lõikel visualiseeruvad paremas hemisfääris hüperehhogeensed selgepiirilised sõlmekesed.
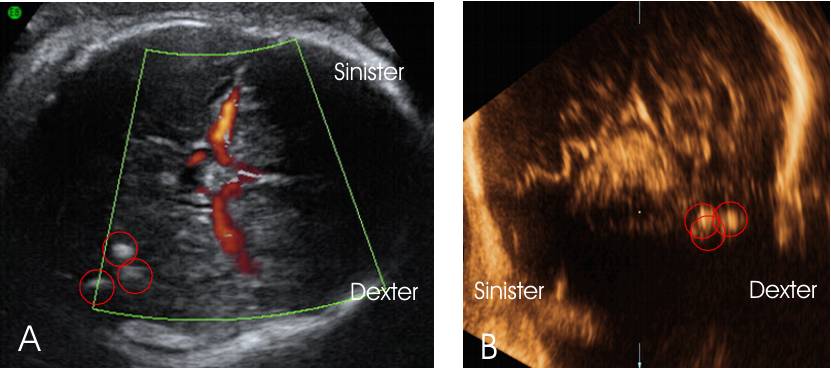
Joonis 2. A: Ultrahelis looteaju aksiaalsel lõikel circulus Willisi tasandil paremas hemisfääris visualiseeruvad hüperehhogeensed kolded. B: Samad kolded visualiseeruvad ka aju koronaarsel lõikel.
Tuberoosse skleroosi kahtlusel tehtud loote aju MRT-uuring, mille alusel lõplikku diagnoosi püstitada ei saanud.
Sünnieelse diagnoosi täpsustamiseks ja sünnieelse jälgimise asjus konsulteeritud prof Rabih Chaoui´ga ning prognoosi ja tulevikuplaanide osas Stanislav Ovroutskiga. 34. rasedusnädalani tehtud 2-nädalase intervalliga loote ehhokardiograafia, jälgides tuumorite kasvu ja pöörates tähelepanu võimalikule südamepuudulikkuse ja rütmihäirete tekkele. Alates 35. rasedusnädalast suunati patsient jälgimisele LTKH Naistekliinikusse. Suurim tumoroosne kolle vasakus vatsakeses kasvas kuni 32. rasedusnädalani, seejärel hakkas vähenema.
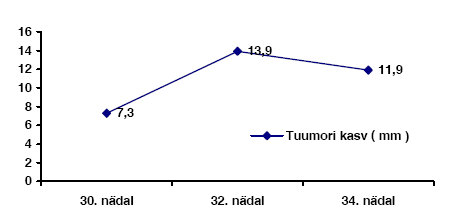
Joonis 3. Suurima tumoroosse kolde kasv vaatlusperioodi jooksul.
Tumoroossetest kolletest ei tekkinud vasaku väljutustrakti obstruktsiooni ega rütmihäireid.
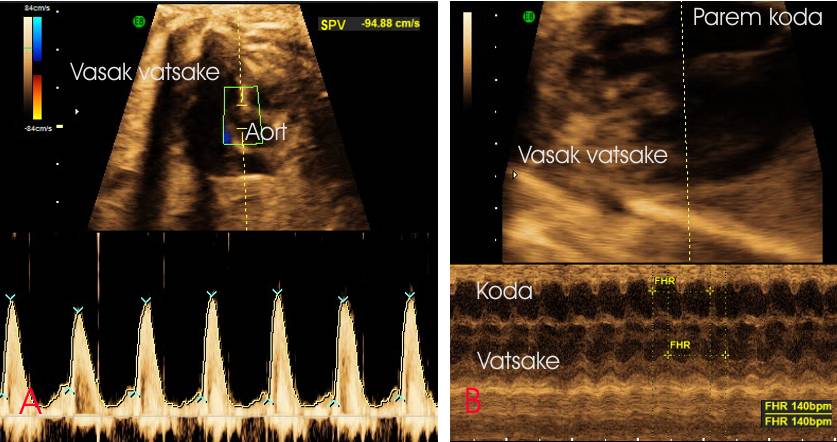
Joonis 4. A: Doppleri signaalikujund aordiklapil 34. rasedusnädalal. Peak systolic velocities (SPV) 94,88 cm/s (95 th 34. rasedusnädalal 110 cm/s). B: Siinusrütmiga lootel südame M-mode salvestus. Kodade ja vatsakeste löögisagedus 140 lööki minutis.
Laps sündis 41. rasedusnädalal (02.02.2010 Lääne-Tallinna Keskhaigla Naistekliinikus) keisrilõike teel loote distressi tõttu, Apgari indeks 6/8/8 palli. Sünnikaal 4548 g, pikkus 58 cm. 6. elupäeval suunati laps edasisteks uuringuteks Tallinna Lastehaiglasse.
Sünnijärgne kliiniline leid lapsel iseärasusteta, nahanähte ei olnud. Ehhokardiograafilisel uuringul kinnitatud hüperehhogeensete kollete leid südame paremas ja vasakus vatsakeses. Südamepuudulikkuse tunnused puudusid. Lapse peaaju MRT-uuringul ilmnesid periventrikulaarsed sõlmekesed ja kortikaalsed tuberkulumid. Neerude ultrahelileid patoloogiata, silmapõhjad muutusteta.
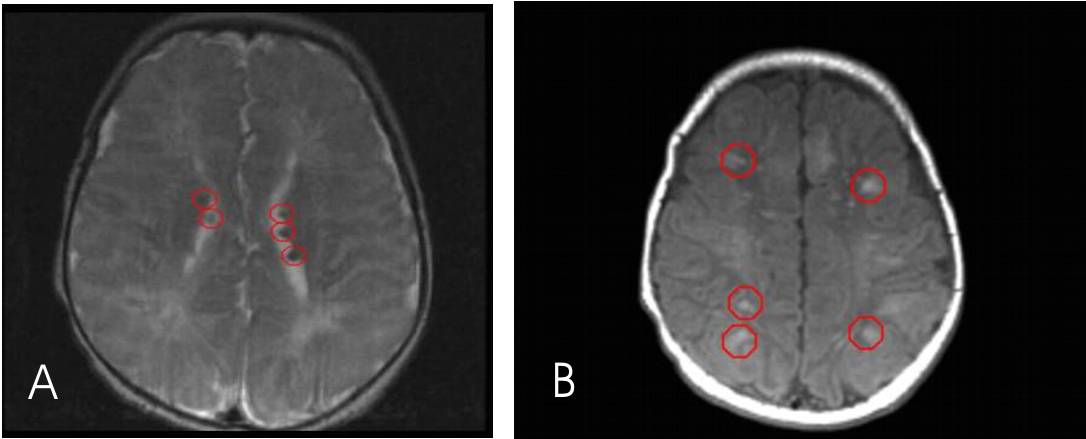
Joonis 5. A: MRT-l ilmestuvad vastsündinu aju aksiaalsel lõikel ajuvatsakestes subependümaalsed sõlmed. B: MRT-l ilmestuvad vastsündinu aju aksiaalsel lõikel mõlemas hemisfääris kortikaalsed köbrud.
Vastavalt tuberoosse skleroosse kompleksi (TSK) kliinilistele kriteeriumitele on patsiendil kolm suurt kliinilist kriteeriumi, mille alusel diagnoositi vastsündinul 8. elupäeval tuberoosne skleroosne kompleks. Geeniuuringu vastus veel tulemata. Hiljem oli laps ambulatoorsel jälgimisel. 2-kuuselt ilmnesid nahanähud tüüpiliste café au lait laikudena ning 3,5-kuuselt krambiavaldused infantiilsete spasmidena; alustatud krambiraviga.
Järeldused
- Makroskoopiliselt normaalne südameleid skriininguuringu ajal ei välista hiljem kliiniliselt väljendunud südamekasvaja olemasolu.
- Loote südame koldeliste muutuste korral on soovitatav uurida ka loote aju. III trimestril on loote aju segmentaalsel ultraheliuuringul võimalik juba üsasiseselt hinnata tuberoosseid subependümaalseid või kortikaalseid koldeid.
- Loote ultraheliuuringu kombineerimine MRT-uuringuga raseduse III trimestril võimaldab täpsustada tuberoosse skleroosi olemasolu. Samas, MRT leiu puudumine III trimestril ei välista TSK olemasolu. [Antenataalse MRT-uuringuga on võimalik avastada 49% sünnijärgselt diagnoositud TSK juhtudest (6)].
- Varajane diagnoosimine võimaldab last võimalike probleemide suhtes hoolikalt jälgida ning alustada vajadusel raviga ja nõustada perekonda. [Neuroloogilised tüsistused ilmnevad 69%-l vastsündinutest, kel oli sünni eel leitud aju MRT, ja 33%-l, kellel MRT leidu polnud (6)].
Südame rabdomüoom
(Rhabdomyoma cordis congenitalis)
Sagedus
Südame kaasasündinud patoloogiatest on südamekasvajaid ligikaudu 2,8%-l juhtudest (4). Rabdomüoom on sagedasim südamekasvaja, 89%-l juhtudest (1), st 0,08%-l vastsündinutest (9). Esimesena kirjeldas sünnieelset südame rabdomüoomi ultraheliuuringul USA günekoloog Greggory DeVore 1982. a (10).
Ultrahelidiagnoos
Südame neljakambrivaatel ilmestuvad 2-dimensioonilisel ultraheliuuringul südame-lihasest lähtuvad üksikud või sagedamini mitmed südamelihasest ehhogeensemad ühtlase ehhogeensusega ovaalsed või ümarad selgepiirilised kolded. Kollete kasvu tõttu võib algul ultrahelis avastatud üksiku kolde kõrvale tekkida hiljem ka teisi koldeid, mis tulevad ilmsiks alles hilisemate ultraheliuuringute käigus. Tuumori läbimõõt on tavaliselt 5–10 mm, kuid on kirjeldatud ka 40-mm koldeid (4). Rabdomüoomid võivad lähtuda nii vatsakeste vaheseinast, külgseintest, südame tipust ning isegi väljutustraktide koonusest. Harvem on neid kodades, papillaarlihastes. Sageli võlvuvad tuumorid südamekambrite poole, põhjustades verevoolu takistusi. Südamest eksofüütselt väljapoole kasvav tuumor on harva rabdomüoom. Rabdomüoome avastatakse tavaliselt 20.–30. rasedusnädala vahel ja nad saavutavad oma kasvus maksimumi tavaliselt 35. rasedusnädalaks. Greipel kaasautoritega on kirjeldanud kahte haigusjuhtumit, kus rabdomüoomid avastati nende väikese suuruse tõttu alles sünnijärgsel ehhokardiograafial (8). Seni pole rabdomüoome diagnoositud raseduse varajases perioodis – 11.–14. rasedusnädalal (2). Kõige varem on kirjanduses kirjeldatud rabdomüoomi 17. rasedusnädalal (7). Sünni järel tuumori maht väheneb oluliselt ja sageli pole teda enam hiljem makroskoopiliselt võimalik hinnata (3). Tõenäoliselt mõjutavad tuumori kasvu ema hormoonid raseduse ajal, mistõttu nad kasvavad raseduse ajal ja vähenevad sünni järel (2, 3, 9).
Diferentsiaaldiagnoos (7)
Sünni eel on südames ainult nelja histoloogilist tüüpi kasvajat: rabdomüoom, teratoom, hemangioom ja fibroom.
- Teratoom. Võib olla nii üksik- kui ka mitmekoldeline. Enamus teratoome lähtub perikardist ning nad on heterogeense struktuuriga (osalt tsüstjad, osalt kaltsifitseerunud alad) ja ehhogeensed. Sageli kaasneb hüdroperikard.
- Hemangioom. Sageli üksikkolletena. Lemmiklähtumiskoht on südamepõhimikul parema koja seinast, võlvudes sageli selle õõnsusesse. Struktuurilt on erisuguse ehhogeensusega. Sageli kaasneb hüdroperikard.
- Fibroom. Paikneb tavaliselt üksikkolletena, lähtudes kas vatsakeste vabast seinast või vaheseinast. Harvem võib tuumoris olla kaltsifikaate või tsüstilist degeneratsiooni. Ehhogeensuselt sarnaneb rabdomüoomidega, kuid erinevalt viimasest esineb alati üksikkoldena.
- Südamesisesed hüperehhogeensed kolded. Difererentsiaaldiagnoos pole raske, sest hüperehhogeensed kolded paiknevad kõõluskeelikutes ja pole kunagi seotud südamelihasega.
Tüsistused
Peamiseks prognostiliseks faktoriks on tuumori maht. Suured rabdomüoomid võivad põhjustada südame sisse- ja väljapääsutraktide obstruktsiooni; südame juhtesüsteemi komprimeerides südame rütmihäireid koos südamepuudulikkuse ja hüdropsiga (3). Huvitav on aga tähelepanek, et vaatamata rabdomüoomide suhteliselt suurtele mõõtmetele ja sellest põhjustatud verevoolutakistusele, on raskeid hemodünaamikahäireid suhteliselt harva ning loote üsasisest surma on kirjanduses küll kirjeldatud, kuid see on pigem erand kui reegel (4–5%-l juhtudest). Ohtlik on olukord, kui tuumorid takistavad koronaarvereringet, see võib lõppeda loote hukuga (2).
Kromosoomipatoloogia risk
Praktiliselt puudub.
Mittekromosomaalsete sündroomide risk
Suur.
Rabdomüoomiga on sageli seotud tuberoosne skleroosne kompleks (TSK, lad sclerosis tuberosa), eriti siis, kui tuumorikoldeid on palju. Hulgikoldeliste rabdomüoomide korral on TSK sagedus 100%; üksikkoldelise vormi korral, kui puudub perekonnaanamnees, 50% (1). 90%-l loodetest, kellel avastati sünni eel rabdomüoomid, areneb TSK alles pärast sündi (3).
Raseduse juhtimine
Kuna kromosoomipatoloogia risk on väike, siis pole karüotüpiseerimine vajalik. Lähitulevikus, kui Eestis avalduvad võimalused TSK molekulaardiagnostikaks, on invasiivsed diagnostilised uuringud omal kohal. Raseduse juhtimine baseerub rabdomüoomide kasvu jälgimises: kui viimased näitavad kiiret kasvu, põhjustades klappide täieliku obstruktsiooni ohu, siis on üks võimalikke lahendusi õigeaegne sünnitus. Südame tahhüarütmia tekkel on üks võimalusi transplatsentaarne digoksiinravi. Kuigi tahhüarütmia, mis on seotud sekundaarselt südame kasvajaga, medikamentoossele ravile sageli ei allu. Laps peaks sündima raviasutuses, kus vastsündinule on võimalik pakkuda vajadusel kardioloogilist abi (3).
Prognoos
85%-l juhtudest rabdomüoomid sünni järel taanduvad, mistõttu medikamentoosne ega kirurgiline ravi pole vajalik. 15%-l juhtudest on vajalik kirurgiline või antiarütmiline ravi. Operatsioonijärgne suremus on väga madal. Pikaajaline prognoos sõltub eeskätt TSK kaasumisest, mille neuroloogiline tulem on sageli prognoosimatu (6). 30%-l juhtudest kaasneb vaimse arengu peetus.
Kasutatud kirjandus
- Smicha Yagel. Fetal Cardiology. Second Edition. Informa Healthcare USA, 2009; 405–408.
- Rabich Chaoui. Paollo Volpe. Alfred Abuhamad. A Practical Guide to Fetal Echocardiography. Second Edition. Lippincott Williams and Wilkins. USA, 2010; 347–350.
- Dario Paladini. Ultrasound of Congenital Fetal Anomalies. Differential Diagnosis and Prognostic Indicators. Informa Healthcare. UK, 2007; 177–179.
- Lindsey D Allan. Fetal Echocardiography. A practical Guide. Cambrige University Press. UK 2009. 66–67; 234.
- R.S. Bader, L.K. Hornberger, J.C.Huhta The Perinatal Cardiology Handbook. Mosby. USA 2009; 341–349.
- J. Saada. Prenatal diagnosis of cardiac rhabdomyomas: incidence of associated cerebral lesions of tuberous sclerosis complex. Ultrasound Obstet Gynecol 2009; 34: 155–159.
- Q. C. Zhou, P. Fan, Q. H. Peng, M. Zhang, Z. Fu and C. H. Wang Prenatal echocardiographic differential diagnosis of fetal cardiac tumors. Ultrasound Obstet Gynecol 2004; 23: 165–171.
- A.Geipel, M.Krapp, U. Germer, R. Becker, U. Gembruch. Prenatal diagnosis of cardiac tumors. Ultrasound Obstet Gynecol 2001; 17: 17–21.
- D. Paladini, S. Palmieri, M. G. Russo, G. Pacileo. Letter to the Editor. Ultrasound Obstet Gynecol 1996 7: 84–85.
- G.DeVore, S. Hakim, C.S. Kleinman, J.C. Hobbins. The in utero diagnosis of interventricular septal cardiac rhabdomyomas by means of real-time-directed, M-mode echocardiography. Am J Obstet Gynecol 1982; 143: 967–969.
- A. Milunsky, M. Ito, T. Maher, et al. Prenatal molecular diagnosis of tuberous sclerosis complex. Am J Obstet Gynecol 2009; 200: 321.e1–6.
- OMIM ( Online Mendelian inheritance in Man )
Summary
Cardiac rhabdomyomas represent the most common lesion of tuberous sclerosis complex in the fetus and may be associated with cerebral lesions such as cortical tubers and subependymal nodules. We present here a case of cardiac multiple rhabdomyomatosis and cortical tubers diagnosed at 30 weeks of gestation in a child with tuberous sclerosis and followed up postnatally to 4 months. To the best of our knowledge this is the first report of tuberous sclerosis complex diagnosed in a fetus and newborn in Estonia.
